BIOFUMIGACIÓN
Y SOLARIZACIÓN COMO ALTERNATIVAS
AL BROMURO DE METILO
A. BELLO, J.A. LÓPEZ-PÉREZ, L. DÍAZ
VIRULICHE
Dpto Agroecología, CCMA, CSIC. Serrano 115 dpdo 28006 Madrid.
antonio.bello@ccma.csic.es
Resumen.
Se estudia la
acción de los gases producidos en la descomposición de la materia
orgánica para el control de nematodos y otros patógenos de origen edáfico.
Su eficacia es similar a la de los fumigantes convencionales. Se
diferencia de la solarización en que no requiere temperaturas
superiores a los 30 ºC, por lo que puede aplicarse en cualquier
estación del año, en áreas donde existen bajas temperatura y en
cultivos extensivos. Por otro lado, la biofumigación actúa en
profundidad resolviendo problemas, como en el caso de los nematodos,
de dinámica vertical, que son comunes en los organismos móviles y
que tienen lugar al aumentar la temperatura del suelo como ocurre con
las técnicas de solarización. Los resultados de la aplicación de la
biofumigación en cultivos extensivos son efectivos en condiciones de
bajas temperaturas y sin aplicación de cubiertas de plástico, a
diferencia de la solarización, aunque ambas técnicas pueden ser
complementarias, e incrementar su eficacia, en el caso de los
nematodos fitoparásitos, cuando se aplican conjuntamente.
INTRODUCCIÓN
Los investigadores y técnicos en
agricultura se están enfrentado a uno de los mayores retos de los últimos
años, el de encontrar alternativas al bromuro de metilo (BM) para
controlar plagas y enfermedades de las plantas. La alternativa que se
proponga debe tener eficacia similar al BM, no impactar sobre el medio
ambiente, ser económica y socialmente viable, características que no han
sido hasta ahora exigidas a ningún otro pesticida. El BM es un biocida
que destaca por su amplio espectro de acción frente a los patógenos de
los vegetales, así como su alta efectividad en cuanto a penetración y
difusión en el suelo, incluso en aquéllos que presentan contenidos de
humedad y temperatura altos. Sin embargo, el BM no se retiene en su
totalidad en el suelo, sino que del 50 al 95 % pasa en
forma
de
emisiones
gaseosas a la estratosfera, donde se liberan
átomos de bromo que reaccionan con el ozono y otras moléculas estables
que contienen cloro, dando lugar a una reacción en cadena que contribuye
a la disminución de la capa de ozono, incrementando la emisión de rayos
ultravioletas con los consecuentes riesgos para la salud y el medio
ambiente (Thomas 1997).
La evidencia científica de la destrucción de la capa de ozono por
el BM, dio lugar a la toma de decisiones que contribuyesen a la retirada
de este producto, apoyándose en acciones reguladoras (UNEP 1992). Así,
algunos países del norte de Europa han eliminado el uso del BM, como es
el caso de Dinamarca, mediante los cultivos sin suelo (Gyldenkaerne,
Yohalem y Hvahøe 1997). Por todo ello, la Unión Europea (UE) ha
propuesto la congelación del consumo de BM, a los niveles de 1991 para
los años 1995-1997 y la reducción de su consumo desde 1998 en un 25 %.
La 10ª Reunión del Protocolo de Montreal estableció, para los países
desarrollados, un programa en el que se acordó la reducción, de forma
gradual, de los usos agrícolas del BM, hasta llegar a su eliminación
total para el año 2005 y para países del Artículo 5º su eliminación
en el año 2015, con una posible revisión para la modificación de la
fecha en el 2003. En la UE, además, ha elaborado un proyecto de
modificación del actual Reglamento en el que se intenta adelantar para el
año 2001 la situación final del BM, aunque las últimas decisiones
mantienen el 2005 como fecha límite, se eliminará el 60% en el 2001 y el
75% en el 2003 (Tierney 1998, 2000). Otros países como Argentina, Brasil,
China, Cuba, Guatemala, Marruecos y Uruguay están elaborando proyectos de
investigación demostrativos para su eliminación total. Respecto a las
alternativas al BM, no existe un único sustituto para todos los usos de
este fumigante del suelo, ya que dependen del organismo patógeno, cultivo
y de la zona, siendo la mejor alternativa los programas de manejo
integrado de cultivos "Integrated Crop Management" (ICM). Para
ello, es importante que las distintas alternativas regulen de forma eficaz
y económica los patógenos controlados actualmente por el BM,
garantizando su viabilidad a largo plazo, Slooteen (1997).
En cuanto al uso de BM en los países con clima mediterráneo, se
estima en alrededor de 24.239 t al año, lo que suponen el 47.6 % del
consumo total, para la fumigación de suelos, siendo España, después de
Italia, el segundo país en consumo (11,7 %) (Fig. 1)(Bello y Tello 1998,
Varés 1998). Actualmente en España la situación es muy diferente debido
a la política de reducción elaborada por el Ministerio de Agricultura,
Pesca y Alimentación (MAPA). Por otro lado, se ha demostrado que puede
reducirse hasta el 50 % la utilización de pesticidas mediante métodos
alternativos con un incremento de sólo el 0,6 % de los gastos de producción
(Pimentel et al. 1993).
La primera impresión sobre la eliminación del BM fue muy
pesimista y, sobre todo, sobre nuestro futuro, puesto que la agricultura y
la capa de ozono son fundamentales para la supervivencia del planeta. Un
análisis posterior nos llevó a la conclusión de que el uso de BM en
agricultura así como los problemas fitopatológicos son la excepción y
no la norma, la inmensa mayoría de cultivos no usan BM (Bello et al.
1994, 1996; Bello, Escuer y Pastrana 1995; Barker y Koenning 1998).
Curiosamente el BM sólo afecta a los cultivos que se han definido como
paradigma de una agricultura moderna, que está localizada principalmente
en California, Florida, España, Japón, Israel e Italia.
Entre los organismos parásitos de plantas que se ven afectados por
la retirada del BM, se encuentran fundamentalmente varias especies de
hongos, los nematodos pertenecientes a los géneros Meloidogyne
y Rotylenchulus, además de los problemas de replantación,
especialmente en frutales.
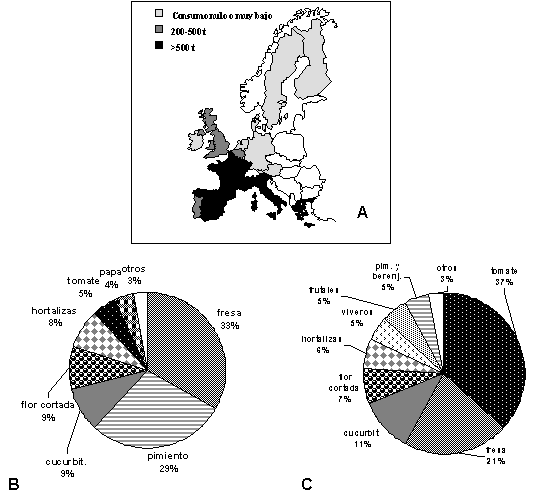
Figura
1. Consumo anual de BM en la UE por países [A] y en España [B] y la UE
[C] por cultivos
Es necesario el uso de criterios ecológicos en agricultura que permitan
conocer cuáles son los elementos y procesos claves en el funcionamiento
de los agrosistemas. En relación con el BM hemos elegido la función de
la materia orgánica a través de los procesos de degradación que
producen gases capaces de controlar los patógenos de los vegetales. Este
proceso ha sido definido como biofumigación (Kirkegaard et al.
1993b; Bello 1998) y ha sido incluido como una alternativa no química al
BM por el "Methyl Bromide Technical Comitte (MBTOC 1997),
perteneciente al Protocolo de Montreal, ampliando a todas las materias orgánicas
y residuos agroindustriales el anterior concepto de biofumigación que se
aplicaba sólo a la emisión de isotiocianatos durante los procesos de
descomposición de las brasicas y su efecto fungicida e insecticida (Kirkegaard
et al. 1993a, b; Matthiesen y Kirkegaard 1993; Angus et al.
1994). Por otro lado, Stirling (1991), en una revisión sobre el control
biológico de los nematodos parásitos de plantas, señala la importancia
de la materia orgánica no solo por mejorar la fertilidad y estructura del
suelo, sino también por su efecto tóxico sobre los nematodos fitoparásitos.
BASES CIENTÍFICAS DE LA BIOFUMIGACIÓN
El concepto "Biological fumigation" fue utilizado por
Kirkegaard et al. (1993a), empleando el término biofumigación
en Kirkegaard et al. (1993b) y Matthiessen y Kirkegaard (1993) y
apareció por primera vez en una revista internacional en Angus et al.
(1994). Recientemente Kirkegaard y Sarwar (1998) definen la biofumigación
como: "the suppression of soil-borne pest and pathogen by brassica
rotation or green manure crops""(Angus et al. 1994;
Kirkegaard et al. 1993a, b).
La biofumigación utiliza los gases y otros productos
resultantes de la biodegradación de las enmiendas orgánicas y residuos
agroindustriales como fumigantes para el control de los organismos patógenos
de vegetales, se contribuye con ello, además, a resolver los problemas
ambientales graves que estos productos pueden producir. Su eficacia se
incrementa cuando se incorpora dentro de un sistema de manejo integrado de
cultivos (Bello 1998) y se diferencia del uso de las enmiendas orgánicas
en las características de los materiales biofumigantes y en el método de
aplicación (Bello et al. 1999b). Esta técnica puede ser de gran
interés en países en vías de desarrollo debido al bajo coste y
facilidad de aplicación (MBTOC 1998). Bello et al. (1999b, 2000a,b,c)
definen la biofumigación como "la acción de las sustancias volátiles
producidas en la biodegradación de la materia orgánica en el control de
los patógenos de las plantas, incrementándose su eficacia cuando se
incluyen en un sistema integrado de producción de cultivos";
presentan resultados de su aplicación en cultivos de cucurbitaceas,
pimientos, zanahoria, tomate, otras hortalizas, fresón, platanera, cítricos,
frutales, viñedos y flor cortada en diferentes ambientes de la región
mediterránea, obteniendo una eficacia similar a los pesticidas
convencionales, al mismo tiempo que incrementan los nematodos saprófagos,
mejoran las características del suelo y la nutrición de la planta, señalando
la necesidad de diseñar una metodología para cada situación, diferenciándose
de la aplicación de la materia orgánica en la dosis y el método de
aplicación.
Fernández, Rodríguez-Kábana y Kloepper (2000) analizan el valor
de los enzimas del suelo para determinar la capacidad de los
microorganismos en la supresión de los patógenos de plantas, señalando
que los contenidos de ureasa y quitinasa están inversamente
correlacionados con el número de nódulos de M.arenaria y que la
aplicación de compost incrementa las poblaciones de bacterias y la
actividad enzimática (ureasa, proteasa, quitinasa, catalasa y la hidrólisis
de diacetato de fluoresceina). Calderón et al. (2000) señalan que
la biofumigación se encuentra entre las mejores alternativas al BM en
cultivos de tomate y brasica en Guatemala. Hewlett y Dickson (2000) señalan
que los nematodos formadores de nódulos (M.arenaria y
M.javanica) pueden ser controlados con la aplicación de taninos.
Bello et al. (2000c) definen la biofumigación, indicando que su
eficacia es similar a la de los pesticidas convencionales, y aunque la técnica
es diferente a la solarización, se pueden complementar incrementando su
eficacia.
Biofumigación
y materia orgánica
La acción de los microorganismos
sobre la materia orgánica durante su descomposición produce gran
cantidad de productos químicos que pueden actuar en el control de los patógenos
del suelo. El amonio, nitratos, sulfídrico y un gran número de
sustancias volátiles y ácidos orgánicos pueden producir una acción
nematicida directa o afectar a la eclosión de los huevos o la movilidad
de los juveniles de nematodos; los fenoles y los taninos son también
nematicidas a ciertas concentraciones (Mian et al. 1982; Mian y
Rodríguez-Kábana 1982 a,b), por ello es difícil determinar con
exactitud qué sustancia es responsable de la muerte de los nematodos.
De todos los productos químicos, obtenidos en la descomposición
de la materia orgánica por la actividad de los microorganismos, que
pueden tener acción nematicida, el amonio ha sido el mejor estudiado,
aunque es difícil afirmar que un solo componente sea responsable de la
mortalidad de los nematodos. La actividad nematicida del amonio fue
reconocida por Eno, Blue y Good (1955), cuando realizaban una serie de
trabajos sobre el empleo de amoniaco anhidro como fertilizante
nitrogenado, al comprobar que aplicado por inyección a la concentración
de 300-900 mg kg-1
de suelo reducía los problemas de nematodos. Experimentos posteriores con
urea, que se convierte en amonio por acción de la ureasa existente en el
suelo, muestran que es un buen nematicida si se aplica en cantidades
superiores a 300 mg de N kg-1
de suelo (Huebner, Rodríguez-Kábana y Patterson 1983).
El contenido de N no es el único factor considerado cuando la
materia orgánica es utilizada como nematicida, el carbono es también
importante, puesto que de él depende la metabolización del nitrógeno
por los microorganismos para convertirlo en proteína y otros compuestos.
En ausencia de fuentes de carbono, el amonio y los nitratos se pueden
acumular y causar fitotoxicidad. Materiales como quitina, urea, algunas
tortas de oleaginosas y nim tienen una relación C/N baja, pudiendo
afectar a las plantas. Se ha demostrado que la materia orgánica con una
relación C/N entre 8-20 tiene actividad nematicida sin efecto fitotóxico
(Rodríguez-Kábana, Morgah-Jones y Chet 1987).
El efecto nematicida tiende a ser limitado a la zona de incorporación,
puesto que el amonio tiene una difusión pobre en el suelo y se mueve sólo
unos pocos centímetros desde el punto de aplicación (Eno, Blue y Goog
1955). El pH del suelo tiene también efecto sobre la eficacia del amonio,
altas concentraciones de amonio son más activas en suelos ácidos que en
alcalinos (Duplessis y Kroontje 1964). Por otro lado, las dosis efectivas
de nitrógeno para el control de nematodos pueden ser fitotóxicas o
contribuir a la contaminación de las aguas subterráneas (Stapleton, de
Vay y Lear 1989).
La cutícula de los nematodos está constituida en material
proteico con una capa de lipoproteínas y la principal estructura de la
cubierta del huevo es quitina, las enzimas de mayor interés son las
enzimas proteolíticas y quitinolíticas. La actividad de la quitinasa
aumenta cuando se añaden al suelo enmiendas que contienen quitina y las
bacterias quitinolíticas tienen capacidad de destruir la cubierta de los
huevos de los nematodos formadores de nódulos (Parker, Haywards y
Stirling 1988). Galper et al. (1991) indican que la adición de colágeno
estimula el desarrollo de las enzimas que actúan sobre la cutícula de
los nematodos.
La quitina es uno de los polisacáridos más frecuentes en la
naturaleza, es tan abundante como la celulosa en los residuos de
fermentación industrial (Gooday 1990). Se ha demostrado el efecto
nematicida de la quitina cuando se aplica en la proporción del 1% (Culbreath,
Rodríguez-Kábana y Morgah-Jones 1985); su acción se debe principalmente
a la producción de amonio durante el proceso de descomposición. La
quitina es un material que contiene nitrógeno y se degrada por hidrólisis,
convirtiéndose en ácido acético y glucosamina, que libera amonio. Uno
de los problemas es su fitotoxicidad, que se puede resolver añadiendo
hemicelulosa y paja, que inmovilizan el exceso de nitrógeno. También se
considera que estimula el desarrollo de la microflora antagonista,
incrementando los actinomicetos.
La adición de materia orgánica al suelo para mejorar la
fertilidad y controlar las plagas y enfermedades es una práctica casi tan
antigua como la agricultura. Se han ensayado una amplia variedad de
materiales como enmiendas al suelo para controlar nematodos, hongos
fitoparásitos y flora arvense. Estos materiales incluyen estiércol de
ganado, residuos de industrias papeleras y forestales, de industrias
pesqueras y de marisqueras, numerosos subproductos de agricultura,
alimentación y otras industrias, así como residuos de plantas con
compuestos alelopáticos (Hoitink 1988; Stirling 1991; Bello 1997; Bello et
al. 1999a,b, 2000b).
Se han ensayado como enmiendas al suelo, para el control de
nematodos y otros patógenos de plantas, materiales con alto contenido en
nitrógeno que generan amoniaco que actúa como un nematicida en el suelo
(Canullo, Rodríguez-Kábana y Kloepper 1992a,b). La adición de quitina o
materiales quitinosos al suelo no sólo genera amoniaco sino también
estimula las actividades de la microflora quitinolítica en el suelo (Rodríguez-Kábana,
Boube y Young 1990). Muchos microorganismos quitinolíticos son efectivos
en la destrucción de huevos de nematodos y micelios de algunos hongos
fitopatógenos. Estos tratamientos pueden contribuir al control de
enfermedades de origen edáfico particularmente cuando se combinan con
otras alternativas, por ejemplo, se ha estudiado la adición al suelo de
enmiendas complementadas con solarización y ofrece un potencial
considerable de incremento de la eficacia de las enmiendas contra los patógenos
con reducción de las cantidades necesarias de materia orgánica por hectárea
(Gamliel y Stapleton 1993).
El mayor problema en el uso de enmiendas orgánicas es la
heterogeneidad en la composición de las materias utilizadas para su
preparación (Stirling 1991). La normalización de la composición de las
enmiendas, control de calidad, es un área de desarrollo que requiere una
metodología apropiada. Algunas enmiendas orgánicas tienen el potencial
para acumular compuestos perjudiciales y aumentar el nivel de inóculo de
algunos patógenos edáficos (Rodríguez-Kábana 1986).
Los nematodos fitoparásitos, por ejemplo, se ven afectados por el
uso de urea y de otras fuentes de nitrógeno amoniacal. Las fuentes de
nitrógeno amoniacal como amoniaco, carbonato amónico y bicarbonato amónico
pueden reducir los efectos producidos por Sclerotinia rolfsii en
zanahoria y otros cultivos (Punja 1985). En algunos casos, solamente se
precisa un cambio de pH para reducir algunas enfermedades del suelo (Cook
y Baker 1983). En Florida Kim, Nemec y Musson (1996a,b) estudian el
compost y la materia orgánica como alternativa al control de Phytophthora
capsici en cultivo de pimiento, encontrando que Quitosan, un
producto que contiene residuos de crustáceos y pulpa de cítricos con
melaza, era efectivo en el control de la enfermedad, incrementado la
actividad biológica del suelo, pudiendo actuar como una alternativa al
BM, debido a la producción de lacasas y peroxidasas, y la acumulación de
ß 1,3-glucanasa, fenoles y la actividad sinérgica entre ß 1,3-glucanasa
y quitinasa. Hoitink (1997) analiza las dificultades que plantea la
utilización de compost como alternativa al BM, señalando que el primer
aspecto es la eliminación de organismos patógenos y malas hierbas, para
ello se deben alcanzar temperaturas superiores a 67 ºC durante varios días,
en segundo lugar puede causar fitotoxicidad debido a la producción de ácidos
orgánicos volátiles como ácido acético, amonio u otros compuestos tóxicos,
por otro lado las altas temperaturas destruyen los agentes de biocontrol,
micorrizas y bacterias promotoras del crecimiento, aunque se puede
recuperar fácilmente a partir de la base del compost que tiene
temperaturas más bajas, se pueden crear problemas de salinidad del suelo
debido al sodio en el estiércol de vaca, por lo que se debe aplicar
varios meses antes de plantar, los compost con alto contenido de nitrógeno
como estiércol y gallinaza puede favorecer enfermedades foliares; y también
pueden crear problemas los compost con contenido de potasio superior a 1%,
que pueden causar problemas de salinidad, en definitiva cada tipo de
compost tiene su propia problemática que debe ser considerada antes de
aplicarse. Tenuta, Hobbs y Lazarovits (1997) estudian los mecanismos
asociados con el control de organismos patógenos con materia orgánica,
indicando que está asociada al NH3,
que se mantiene durante 4 días en suelos arenosos y en los arcillosos se
mantiene el 60%. Allen et al. (1997) encuentran que la anaerobiosis
creada por inundación en combinación con compost durante 12 semanas
controla Meloidogyne arenaria en hortalizas en Florida, demostrando
que los nematodos no sobreviven después de dos semanas de anaerobiosis. Díaz-Viruliche
et al. (2000) estudian el efecto biofumigante de diferentes abonos
verdes de plantas representativas de crucíferas, cucurbitáceas, gramíneas
y leguminosas, encontrando una eficacia superior al 90 % en el control de M.
incognita, estudiando el efecto biomejorador de los biominerales
encontrados en las plantas estudiadas.
Biofumigación y control de nematodos
La mayoría de las publicaciones
existentes sobre la aplicación de la biofumigación propiamente dicha en
el control de nematodos fitoparásitos corresponden a nuestro equipo de
Nematología Agraria (Bello et al. 2000). Por otra parte, existe
gran número de excelentes trabajos sobre el empleo de enmiendas orgánicas,
abonos verdes y residuos agroindustriales, especialmente en países como
Egipto, India y Pakistán, así como de modo aislado en Latinoamérica.
En el Congreso de la Organización de Nematólogos de los Trópicos
Americanos (ONTA), que tuvo lugar en San Juan de Puerto Rico en junio de
1999, aparecen por primera vez algunas comunicaciones, que pueden
considerarse con enfoque científico, que entran dentro de los conceptos
que hemos planteado sobre biofumigación. Así Rodríguez-Kábana (1999)
presenta un biofumigante, que está en fase de patentar, que controla M.
incognita y flora arvense; Bello, Escuer y Tello (1999) aplican con
eficacia la biofumigación en el control de M. incognita y Rotylenchulus
reniformis en Guatemala; Arias et al. (1999), al estudiar las
alternativas al BM en una rotación pepino-acelga en invernaderos de la
Comunidad de Madrid, afectada fundamentalmente por M. incognita,
utilizan compost de champiñón (5 kg m-2),
observando una disminución de las poblaciones del nematodo y un
incremento de la producción en las parcelas con tratamiento de compost;
Bello et al. (1999a) señalan la eficacia del empleo de la
biofumigación en el control de nematodos en Guatemala y Uruguay;
Quiroga-Madrigal et al. (1999) estudian el efecto de canavalia,
crotalaria y mucuna sobre la actividad enzimática del suelo; Rubiano-Rodríguez
y Vargas-Ayala (1999) utilizan Mucuna deeringiana en el control de Meloidogyne,
Pratylenchus y Radopholus en Puerto Rico.
Biofumigación y control de hongos
Destacan principalmente los
trabajos que, bajo el término de biofumigación, han venido
realizando investigadores del CSIRO de Australia desde 1993 para el
control de hongos, puesto que la bibliografía sobre la función de la
materia orgánica, los abonos verdes y los residuos agroindustriales y su
relación con los hongos del suelo es muy abundante y, por lo general, los
trabajos no han sido realizados teniendo en cuenta su efecto biofumigante.
Papavizas y Davey (1960) observan que abonos verdes de trigo, maíz,
avena, guisante y pastos de Sudán controlan Rhizoctonia solani en
judías. Chan y Close (1987) encuentran que la incorporación de crucíferas
al suelo inhiben el desarrollo del hongo Aphanomyces en guisante,
aunque no determinan las sustancias responsables. Kirkegaard et al.
(1993a,b), Angus et al. (1994) y Kirkegaard et al. (1994)
demuestran que las sustancias volátiles de las brasicas inhiben el
crecimiento del hongo del trigo Gaeumannomyces graminis,
demostrando que el efecto biofumigante se debe a los isotiocianatos. Walia,
Mehta y Gupta (1994) estudian el efecto de los residuos del nim (Azadirachta
indica) y del bambú (Leucaena leucocephala) en el control de M.
incognita que, reduce sus poblaciones, y el nim además las de los
hongos Rhizoctonia bataticola y R.solani. Oliveira et al.
(1996) encuentran que fracciones proteícas obtenidas de Cannavalia
ensiformis inhiben el crecimiento de los hongos Macrophomina
phaseolina, Colletothricum gloesporioides y Sclerotium rolfsii. Vulsteke
et al. (1996) señalan el interés del abono verde en el control de
Pythium violae en zanahoria en Bélgica, considerándolo
responsable del "cavity spot" de la remolacha. Candole y
Rothrock (1997) encuentran que el abono verde de Vicia villosa en
un cultivo de algodón reduce a Thielaviopsis basicola encontrando,
en estudios in vitro y en campo, que la supresión se debe a un
producto volátil, el amonio, que se produce a los 3-7 días después de
la incorporación, siendo más sensible al amonio T.basicola que Rizocthonia
solani o Pythium ultimum. García y Poot (1997) utilizan estiércol
de vaca en el control de las enfermedades del aguacate en México.
Kirkegaard y Sarwar (1998) revisan la biofumigación con abonos verdes de
brasicas, definiéndola como: "la supresión de organismos del suelo
patógenos de plantas y otros patógenos por compuestos biocidas
originados de la hidrólisis de los glucosinolatos producidos durante la
descomposición de los abonos verdes de brasicas". El efecto de las
brasicas en el control de los organismos patógenos ha sido revisado por
Brown y Morra (1997) y Rose, Heaney y Fenwick (1997). El término
biofumigación ha sido empleado muy recientemente para la supresión de
los organismos patógenos de los vegetales con rotación o abonos verdes
de brasicas (Kirkegaard et al. 1993; Angus et al. 1994) y su
interés va en aumento en horticultura ante la retirada de varios
pesticidas de síntesis y fumigantes del suelo como el bromuro de metilo.
Se ha encontrado en cereales que con residuos de Brassica napus y B.juncea
se controlan los hongos del suelo (Angus, van Herwaarden y Howe 1991;
Kirkegaard, Wong y Desmachelier 1996; Sarwar y Kirkegaard 1998; Sarwar et
al. 1998); señalan que la eficacia de la biofumigación depende de
varios factores, pero fundamentalmente de la brasica empleada, pero además
de la eficacia en la incorporación de los abonos verdes, la actividad
enzimática de la mirosinasa que
es responsable de la hidrólisis de los glucosinolatos, a las pérdidas
por volatilización, la absorción por la arcilla, la pérdida por
percolación y la degradación microbiana (Brown y Morra 1997). Sarwar y
Kirkegaard (1998) estudian las implicaciones del ambiente en la optimización
de la biofumigación, encontrando que es eficaz a 12 - 20 °C en
invernadero, que el contenido de glucosinolatos aparece relativamente
constante a las diferentes condiciones ambientales y estados de
crecimiento de la planta, disminuyendo el contenido desde el inicio de la
floración, no encontrándose grandes diferencias entre las raíces y la
parte aérea, la excepción fue que Brassica campestris tiene una
mayor cantidad de glucosinolatos durante la floración. Se observa que la
incidencia del ambiente sobre el desarrollo fenológico y la producción
de biomasa puede interferir en la eficacia de la biofumigación, de ahí
la importancia de conocer la influencia del ambiente.
El abono verde de brasica se ha considerado supresor de organismos
productores de plagas y enfermedades cuando se incorpora al suelo (Chan y
Close 1987; Mojtahedi et al. 1991). Este efecto se atribuye por lo
general a compuestos biocidas como los glucosinolatos, que por hidrólisis
dan lugar a sustancias como isotiocianatos, que se han considerado como
los productos más tóxicos (Brown y Morra 1997; Rose, Heaney y Fenwick
1997). El término biofumigación es un concepto de uso reciente en el
control de los patógenos vegetales con abonos verdes de brasicas (Kirkegaard
et al. 1993; Angus et al. 1994) y se considera una
alternativa al BM y dibromide etileno en la supresión de hongos patógenos
(Kirkegaard, Wong y Desmarchelier 1996). Se ha encontrado que las
condiciones climáticas, edáficas y bióticas influyen en la concentración
de glucosinolatos (Rose, Heaney y Fenwick 1997), aunque hay que tener en
cuenta que la luminosidad y temperatura influyen en la fenología de la
planta y en la producción de biomasa (Nanda et al. 1996).
Kirkegaard y Sarwar (1998) señalan que el período óptimo es a la mitad
de la floración y estudia 76 variedades y especies diferentes de Brassica.
Estos resultados de máxima concentración coinciden con la época de
floración, habiendo sido obtenidos por Fieldsend y Milford (1994). Sarwar
et al. (1998) investigan el efecto de la biofumigación con
brasicas sobre el crecimiento de 5 patógenos de los cereales: Gaeumannomyces
graminis var. tritici, Rhizocthonia solani, Fusarium
graminearum, Bipolaris sorokiniana y Pythium irregulare. De
ellos, Gaeumannomyces es el más sensible a los tratamientos,
seguido por Rhizoctonia y Fusarium, siendo Bipolaris
y Pythium los menos sensibles. Se demuestra así el efecto en el
control de hongos de los cereales.
Las brasicas contienen compuestos conocidos como glucosinolatos (Kjaer
1976) que cuando se hidrolizan por la acción del enzima mirosinasa dan
lugar a isotiocianatos. Los resultados de la hidrólisis dependen de las
condiciones ambientales (Rosa, Heaney y Fenwick 1997), los glucosinolatos
son inactivos contra microorganismos, pero los productos de hidrólisis
son biocidas muy eficaces contra nematodos, bacterias, hongos, insectos y
la germinación de semillas (Brown y Morra 1997; Rosa, Heaney y Fenwick
1997; Smolinska et al. 1997). Como la mayoría son volátiles (Kirkegaard,
Wong y Desmarchelier 1996), se utiliza el término biofumigación. Los
efectos sobre el control de hongos han sido señalados por Walker, Morrell
y Foster (1937). Se ha demostrado que la hidrólisis de
glucosinolatos a isotiocianatos en suelo es baja, de un 15% (Borek et
al. 1997). Bowers y Locke (1997) estudian el efecto de extractos de trébol,
nim, pimiento y cassia sobre Fusarium oxysporum f. sp. chrysanthemi,
encontrando que al 10% de emulsión se reduce la densidad del hongo, e
incluso a un 5% para los extractos con nim, con una eficacia para
pimiento, trébol y cassia de 99.9, 97.5 y 96.1 respectivamente, a los
tres días de su aplicación, aunque el hongo se recupera rápidamente.
Hunter et al. (1997) utilizan compost de champiñón en el control
de Cylindrocladium scoparius en viveros forestales. Sams, Charron y
Chordonnet (1997) usan residuos de brasicas en el control de Botrytis
cinerea, indicando que Urbasch (1984) había aislado los productos
responsables del control de B.cinerea, Rhizoctonia solani, Fusarium
oxysporum, Didymella lycopersici y Clamisdosporum fulvum.
Tjamos (1999) en Grecia, al estudiar el interés de la solarización como
alternativa al BM, señala que ésta puede mejorar cuando se añade
materia orgánica, encontrando que combinando solarización y biofumigación
se puede controlar Sclerotinium cepivorum, utilizando 1 kg m-2
de gallinaza. Elena, Paplomatas y Petsikos-Panayotarou (1999) utilizan
como abono verde Lolium perenne y Triticum vulgare en el
control de Fusarium proliferatum y F.oxysporum f.sp.asparagi
en Grecia, considerando que se debe a fenómenos de anaerobiosis.
Villeneuve y Lepaumier (1999) estudian el efecto de la incorporación de
la materia orgánica en el control de Fusarium oxysporum f.sp. asparagi,
Rhizocthonia solani, Sclerotinia sclerotium, Verticillium dahliae,
Meloidogyne spp. y Pratylenchus spp., indicando que estos
resultan sensibles al tratamiento, que denomina biodesinfectación,
pero, si se considera que esta técnica permite la reducción del empleo
de los fumigantes, están hablando de una biofumigación. En este
trabajo señalan que la fermentación de la materia orgánica provoca una
modificación de la atmósfera del suelo incrementando el CO2
y disminuyendo el O2,
dando lugar a fenómenos de anaerobiosis, consiguen de 90-100% de reducción
de patógenos (Blok et al. 1998) cuando se emplea brasicas y
gramineas, al mismo tiempo que aportan microorganismos exógenos al suelo;
resultando que es más eficaz cuando se cubre el suelo con plástico negro
que con transparente y que las brasicas al producir isotiocianatos volátiles
son más eficaces que los metil-isotiocianatos que se obtienen en la
degradación del metam sodio (Brown y Morra 1997), otras plantas de interés
es el sorgo (Sorghum bicolor o S.sudanense) que
contiene compuestos de cianídrico. Estos métodos se pueden combinar con
la solarización en determinadas épocas del año. Los factores
ambientales influyen sobre la calidad y cantidad de glucosinolatos y los
compuestos cianídricos (Rose, Heany y Fenwick 1997), recomiendan
tratamientos de 40 t ha-1
de materia orgánica y en el caso de las brasicas de 65 a 82 t ha-1,
y sembrar 20 kg de semillas por hectárea.
Duniway et al. (1999) en fresón en California encuentran
que la materia orgánica con alto contenido de nitrógeno, restos de
sangre, plumas y restos de pescado, 8, 4 y 8 toneladas respectivamente,
reduce la incidencia de Verticillium dahliae cuando se incorpora 7
semanas antes de plantar. Otara y Ndalut (1999) encuentran que un extracto
de hojas de Conyza floribunda (Asteraceae) controla el Fusarium
oxysporum in vitro. Gamliel et al. (1999) encuentran que
los propágulos de Fusarium oxysporum f.sp. basilici,
Sclerotinium rolfsii y Pythium ultimum se reducen en más del
95 % cuando se someten a solarización más materia orgánica con alto
contenido de nitrógeno, mejorando el control de los patógenos cuando se
combina el tratamiento del suelo con una rotación con trigo. Tenuta y
Lazarovits (1999) estudian los mecanismos de control de los patógenos
vegetales por materia orgánica con alto contenido de nitrógeno,
concluyendo que es una alternativa al BM para determinados suelos, indican
que debe ser estudiada la proporción de materia orgánica en cada suelo y
campo en concreto, que el contenido de nitrógeno en la materia orgánica
debe ser superior a 8% alrededor de 1.600 kg N ha-1
o más de 20 t ha-1
de materia orgánica, siendo letal a los 4-14 días después de
incorporado, por lo que se debe plantar después de 1-2 meses de la
aplicación. Se demuestra que controla Verticillium dahliae,
Streptomyces scabies, Fusarium oxysporum f. lycopersici y Sclerotinia
sclerotiorum en papa. Los experimentos se han mantenido a 24 ºC,
siendo más eficaz en los pH superiores a 8,5 duplicando la eficacia
cuando el pH es superior a 6.
Biofumigación
y control de insectos
Matthiessen y Kirkegaard (1993)
emplean el término biofumigación al tratar de sustituir el uso
del metam sodio en el control de Graphognathus spp. ("whitefringed
weevil") de la papa en Australia, puesto que este producto tiene un
amplio espectro de actividad no sólo sobre los organismos causantes de
plagas y enfermedades sino también sobre muchos organismos beneficiosos.
Estos efectos negativos les hace dudar de la sustentabilidad del metam
sodio a largo plazo. Por otro lado, indican que el metam sodio es muy caro
y debe ser aplicado cuidadosa y correctamente. Estos autores señalan que
su componente activo es el metil isotiocianato (ITC's), un compuesto volátil
que se produce sintéticamente por la industria química, sin embargo
existen otras fuentes naturales, no solo del metil isotiocianato, sino de
otras formas de isotiocianatos (ITC's). Estas fuentes de ITC's se
encuentran principalmente en diferentes especies y variedades de brasicas,
entre ellas las col, coliflor, mostaza y nabo.
Los estudios realizados han demostrado que los ITC's producidos por
las brasicas tienen efecto repelente sobre el "gusano de
alambre", aumentado su eficacia cuando estos insectos están en fases
tempranas de crecimiento, puesto que tienen menor tamaño y son más
susceptibles a los tóxicos. Cuando los huevos del insecto Graphognathus
spp. ("whitefringed weevil") eclosionan, en el Este de
Australia, después de las primeras lluvias de otoño, son muy pequeños
(1 mm de longitud), en lugar de crecer y desarrollarse rápidamente, las
larvas permanecen en el primer estadio durante muchas semanas debido a las
bajas temperaturas del invierno. El crecimiento sólo aparece cuando
aumenta la temperatura en primavera. Por todo ello las larvas de este
insecto pueden ser controladas por biofumigación antes de plantar papas.
En otros casos, las brasicas pueden actuar como repelentes. El concepto
de biofumigación ha estado más relacionado con los organismos patógenos
de origen edáfico, siendo nueva esta idea de que puede controlar
insectos. Elberson et al. (1996), Borek et al. (1997) y
Noble y Sams (1999) encuentran que la biofumigación con concentraciones
altas de Brassica juncea puede controlar larvas de diferentes
especies de insectos, incorporando una biomasa de 4 y 8% de suelo.
Biofumigación
y control de flora arvense
La aplicación de las técnicas de
biofumigación en el control de la flora arvense no tienen el mismo
desarrollo que en el de nematodos, hongos e insectos, con la excepción de
los proyectos que UNIDO, dentro del Protocolo de Montreal, viene
desarrollando como alternativas al BM en países del Artículo 5, donde se
han obtenido resultados altamente positivos, que no están aún
publicados. Sin embargo son numerosos los trabajos existentes con alelopatías
y su interés en el control de la flora arvense, que hasta cierto punto
tienen que ver con la biofumigación, pero, sobre todo, cuando se revisan
los Weed Abstracts fundamentalmente en el apartado de técnicas
culturales, se encuentran algunos trabajos sobre el uso de materia orgánica
y abonos verdes, que nos permite afirmar que la biofumigación puede ser
una alternativa en el control de la flora arvense.
Aponte, Pérez y Tablante (1992) en Venezuela estudian el control
de malezas y enfermedades del tomate con la utilización de residuos de
cosechas. Pandey (1994a,b) encuentra en la India que los residuos de hoja
de Parthenium hysterophorus inhiben el crecimiento de Salvinia
molesta, señalando el interés del trabajo para comprender la dinámica
de poblaciones de la flora arvense en los sistemas acuáticos naturales.
Edwards, Walker y Webster (1994) estudian el efecto de residuos orgánicos
no compostados, con una relación C:N = 30:1, que se modifica al añadirle
gallinaza, en algodón en el Norte de Alabama (EE.UU.), encontrando que la
utilización de estos residuos con cubiertas de paja de trigo reduce la
flora arvense durante el invierno, no habiendo diferencia entre los
tratamientos químicos o no químicos; señalando que los residuos con
celulosa tienen gran valor potencial para el manejo del suelo en
agricultura. Cloutier, Marcotte y Leblanc (1994) estudian el potencial de
80 especies o variedades para ser utilizadas como abono verde en el
control de malas hierbas en Canadá, encontrando que las crucíferas son
las más eficaces y en segundo lugar algunas gramíneas como trigo, cebada
y avena, y entre las leguminosas, el guisante. Hintzsche y Pallutt (1995)
desarrollan un programa de producción integrada donde incluyen abonos
verdes para el control de la flora arvense en Alemania. Mathew y Alexander
(1995) estudiaron el efecto del abono verde en el control de la flora
arvense en arroz en India. Boydston y Hang (1995) estudiaron el efecto del
abono verde de Brassica napus en el control de la flora arvense en
papas EE.UU., encontrando que si se incorporan en primavera, la densidad
de la flora arvense se reduce un 73 a 85 %, el abono de nabos se añadió
a suelo franco arenoso a 20 g de materia verde por 400 g de suelo. Dyck,
Liebman y Erich (1995) demuestran que el uso de abono verde de leguminosas
(Trifolium incarnatum) producen una considerable reducción de
herbicidas y fetilizantes de síntesis en EE.UU. J.M. Zhao y F. Zhao
(1995) estudian el manejo del suelo en cultivos de manzana en China, señalando
la importancia de las cubiertas orgánicas y los abonos verdes. Abdel-Samie
y El-Bially (1996) estudian el efecto de Azolla en la supresión de
la flora arvense en arroz en Egipto, indicando que fue tan eficaz como
cuando se efectúan dos arranques a mano. Álvarez et al. (1996)
utilizan Cannavalia ensiformis como abono verde para controlar
malas hierbas en cultivos de Xantomonas en Cuba. Nietschke (1996)
en el Sur de Australia revisa los métodos de control de avena loca, señalando
el interés de los abonos verdes. Al-Khatib, Libbey y Boydston (1997)
estudian el efecto supresor de los abonos verdes de brasicas (Brassica
hirta), centeno o trigo en el control de la flora arvense en cultivos
de guisante, encontrando que las brasicas añadidas al suelo a las dosis
de 20 g por 400 g de suelo seco reduce la emergencia de Capsella bursa-pastoris,
Kochnia scoparia y Sestaria viridis en un 97, 54 y 49 %
respectivamente. Beltrán
(1997) revisa los efectos alelopáticos y sus mecanismos estableciendo métodos
para el control de la flora arvense. Ciuberkis (1997) encuentra que el
estiércol reduce la flora arvense en Lituania. Edwards y Walker (1997)
estudiaron el uso de residuos orgánicos, incluidos los urbanos, en el
control de la flora arvense en algodón en EE.UU. Kim Kilung y Park
Kwangho (1997) revisan los componentes alelopáticos aislados de plantas
cultivadas, que tienen alto potencial para el control de la flora arvense,
especialmente en arroz, remolacha, altramuz, maíz, trigo, avena,
guisante, cebada, centeno y pepino. Li Shanlin et al. (1997)
estudian en China el efecto herbicida de los
extractos de trigo y sugieren que se debe a varias sustancias entre ellas
el etanol. Webston, Nimbal y Czarnota (1997) aíslan productos naturales
de Sorghum bicolor que son fitotóxicos sobre determinada flora
arvense. Quarles (1997) aísla una sustancia herbicida del gluten de maíz.
Anju Kamra y Gaur (1998) encuentran que la solarización aplicada en un
período de tres a seis semanas y combinada con estiércol reduce los
problemas de nematodos, hongos y flora arvense, con la excepción de Cyperus
rotundus. Dhanapal et al. (1998) utilizan extractos de nim, Ricinus
communis y mostaza en el control de Orobanche. Eberlein et
al. (1998) estudian el efecto supresor para la flora arvense de varios
cultivares de Brassica napus utilizados como abono verde debido a
los glucosinolatos existentes en sus raíces, que actúan como
biofumigantes, señalan que la eficacia depende del cultivar. Golpa
Krishnan, Holshouser y Nissien (1998) utilizan abono verde de brasicas
para la supresión de la flora arvense. Yang, Kim y Chung (1998) estudian in
vitro el efecto alelopático del extracto de arroz, cebada, avena,
centeno y trigo, y encuentran que el alcohol metílico que se encuentra en
estos extractos inhibe la germinación de 6 especies de flora arvense: Amaranthus
retroflexus, Chenopodium album, Arthraxon hispidus, Digitaria adscendens,
Echinochloa crusgallia y Setaria viridis, además en campo
mejoran la producción del cultivo de Ging-seng. Rosskopf, Chellemi y
Kokalis-Burelle (1999) estudian el efecto de la solarización con compost
en el control de la flora arvense en hortalizas de Florida, indicando que
los resultados son comparables al BM.
Biofumigación
y control de bacterias, virus y postcosecha
En este apartado se dan algunos
datos sobre la posible aplicación de la biofumigación en el control de
bacterias, virus y postcosecha, tema de investigación que se viene
desarrollando especialmente en los últimos años.
Bacterias. La aplicación de materia orgánica produce un
incremento de nematodos saprófagos, que reducen la incidencia de las
bacterias patógenas de los vegetales, en este sentido conviene señalar
que Ryder y Bird (1993) encuentran que el nematodo saprófago Acrobeles
nanus reduce los problemas de Restonia corrugata, indicándonos
el valor de la biofumigación en el control de las bacterias, puesto que
los nematodos se duplican en los suelos biofumigados. Akiew, Trevorrow y
Kirkegaard (1996) estudian el efecto de mostaza y residuos de tabaco en la
reducción de Restonia solanacearum en tomate. Michel y New (1996)
encuentran que la materia orgánica con urea (200 kg N ha-1)
y CaO (5.000 kg ha-1),
reduce las poblaciones de Restonia solanacearum dependiendo del
tipo de suelo, siendo efectivo en suelos básicos. Lazarovits, Conn y
Kritzman (1997) encuentran que los residuos orgánicos con alto contenido
de nitrógeno reducen las poblaciones de Verticillium dahliae, la
bacteria Streptomyces scabies, nematodos y malas hierbas en papa,
sin embargo puede producir efectos fitotóxicos en el primer cultivo,
aunque el estiércol de cerdo, el estiércol de vaca y algunos compost sólo
reducen la bacteria, indicando que esto depende de la especificidad del
suelo y de la dosis. Se han encontrado resultados similares en tomates y
frutales, considerando que la materia orgánica es un buen candidato para
reemplazar el BM, especialmente en suelos arenosos, durando su capacidad
biocida varios años y siendo más económico que el BM, al mismo tiempo
que incrementa los organismos del suelo. Michel et al. (1997)
encuentran efecto supresivo en el abono verde de soja, caupí o residuos
de cebolla adicionándole 200 kg ha-1
de nitrógeno ureico y 500 kg ha-1
de CaO reduciendo las poblaciones de R. solanacearum en tomate,
parece que el efecto supresor se produce durante la trasformación de la
urea en presencia de CaO.
Virus. La biofumigación puede actuar indirectamente, sobre
virus al eliminar hongos, nematodo e insectos vectores. Jacobs et al.
(1994) señalan la actividad nematicida, antiviral, antifúngica y
antibacteriana de Tagetes patula y T.erecta. Se ha observado
en los experimentos de campo que hemos realizado que la incidencia de
virus es nula.
Postcosecha.
Se ha realizado la aplicación del biogas obtenido de la fermentación de
plátanos en la conservación de maíz en Nicaragua, obteniéndose una
eficacia del 95 % en el control del gorgojo del maíz (Sitophilus
zeamais) (Lacayo et al. 1996).
BIOFUMIGACIÓN
Y SOLARIZACIÓN
Katan (1981) sugiere que la adición
de residuos orgánicos al suelo puede incrementar la eficacia de la
solarización. Pullman et al. (1981) indican que la solarización
reduce Verticillium dahliae a profundidades de 70-120 cm,
consideran que se debe a los gases liberados durante el proceso de
solarización, puesto que a esa profundidad la temperatura no tiene efecto
letal. Horiuchi et al. (1982) observan que la eficacia de la
solarización es mayor cuando se incorporan abonos verdes de nabo. Kodama
y Fukui (1982) señalaron que
es conveniente añadir almidón soluble al medio, 25-30 g kg-1
de suelo seco, para aumentar el efecto de la solarización. Stapleton y de
Vay (1986) indican que la reducción de nematodos a profundidades entre
46-91 cm en California se debe a otros factores diferentes de la
temperatura. Munnecke (1984) indica que la solarización es eficaz en el
control de Fusarium oxysporum, cuando se añaden coles, debido a
los gases fitotóxicos que se producen en su descomposición.
Garibaldi y Gullino (1991) revisan el empleo de la solarización en
los países del sur de Europa, indicando que crea vacío microbiológico y
no hay eficacia en aquellas capas donde no llega la radiación solar
(30-40 cm), puesto que la solarización se basa en el calentamiento del
suelo de 36 a 50 °C y ésto sólo ocurre en los primeros 30 cm. Katan y
de Vay (1991), en el epilogo de un libro sobre solarización, después de
revisar los problemas que se han planteado los investigadores sobre
solarización en los 15 últimos años, indican que el futuro del método
de solarización está en el uso de plásticos degradables, mejorar la
eficacia de la coberturas, encontrar nuevas vías de aplicación de la
solarización en el control de los patógenos en el material de propagación,
descontaminación del suelo de pesticidas, reducción de la salinidad, y
desarrollo de modelos de producción que permitan su aplicación en
regiones y períodos fríos del año. De Vay y Katan (1991) indican que
existen muchas preguntas sobre la solarización que no tienen respuestas,
tales como si el control de los organismos fitoparásitos es posible a
profundidades comprendidas entre 60-120 cm en suelos solarizados, cuando
la temperatura total necesaria no se alcanza a esa profundidad, y la
posible función de las sustancias volátiles en la reducción de los patógenos.
Tjamos (1998) hace una excelente revisión de la solarización en los países
del Sur de la UE, indicando que es una buena alternativa al BM que incluso
puede eliminar bacterias como Clavibacter michiganensis (Antoniou,
Tjamos y Panagopoulos 1997a,b), aunque los hongos Monosporascus sp.,
Macrosphmina phaseoli y Fusarium oxysporum f. sp. dianthi
no son fácilmente controlados por solarización (Elena y Tjamos 1992). Se
ha considerado que aumentan hongos y bacterias antagonistas
termotolerantes induciendo fungistasis después de la aplicación de la
solarización, entre ellos Talaromyces flavus y Aspergillus
tenuis (Tjamos, Biris y Paplomatas 1991), T.flavus que en
presencia de glucosa, la glucooxidasa produce hidrógeno peroxidasa que es
letal para los propágulos de Verticilium dahlia (Fravel 1988; Kim,
Fravel y Papavizas 1988). Stapleton y de Vay (1984) estudian el efecto de
la solarización del suelo sobre las bacterias demostrando el efecto
beneficioso sobre las especies termófilas de los géneros Actinomices,
Bacillus y Pseudomonas que producen antibióticos que reducen
las poblaciones del suelo, incrementando las bacterias pectolíticas que
favorecen la anaerobiosis. Gambiel y Katan (1991) encuentran efecto
beneficioso de la solarización sobre el incremento y supervivencia de Pseudomonas
fluorescens y P.putida. Señalar, por último, que el principal
problema de la solarización es el período de duración, por lo que sería
de interés optimizar el método con la introducción de bajas dosis de
fumigantes y organismos antagonistas, combinando la solarización con
agentes de biocontrol, o introducir la supresividad del suelo (Greenberger
et al. 1987; Katan, de Vay y Greenberger 1989; Katan, Fishler y
Grinstein, 1983). Blok et al. (1998) estudian en laboratorio el
efecto sobre el control de Fusarium oxysporum f. sp. asparagi
de cinco materiales vegetales diferentes: Lolium perenne, Brassica
oleracea convar oleracea var gemmifera, restos de
cultivos, frutales y residuos de jardín compostados, paja de trigo (Triticum
aestivum) y alfalfa (Medicago sativa), que fueron cortados en
trozos pequeños de aproximadamente 0,5 cm2,
aplicando 70 g de peso seco a 100 ml de un suelo franco arenosos con pH
7,5 y un contenido de materia orgánica del 3,3%, se introdujo en botellas
de vidrio incubándolo a 11 y 24 ºC, encontrando que el consumo de oxógeno
fue mayor a 24 ºC y que después de 7 semanas no se detecta el hongo en
los tratamientos con alfalfa y brasica. Posteriormente se repitio el
experimento en campo durante el verano de 1994 y 1995 utilizando solo Brassica
oleracea convar. botrytis var. cymora y Lolium
perenne, en parcelas experimentales cubiertas con plástico y sin plástico,
estudiando su efecto sobre F.oxysporum f. sp. asparagi,
Rhizoctonia solani y Verticillium dahliae a 15 cm de
profundidad en suelo franco arenoso que en el verano de 1994 presenta un
pH 6,1 y un contenido de materia orgánica del 31%, aplicando 135 kg N,
240 kg K2O
y 160 kg MgO ha-1,
se añadieron las plantas de 4 semanas con un peso fresco de 3,8 kg m-2
para las brasicas y 4 kg m-2
para Lolium, se incorporó con un rotavator a una profundidad de
20-25 cm y se regó con un aspersor durante toda una noche y se cubrió
con plástico. El segundo año (1995) el suelo presentaba un pH 6,5 y un
contenido de materia orgánica del 3,4 %, se aplicaron 3,4 kg y 4,0 kg m-2
de peso fresco para el brócoli y Lolium respectivamente, actuando
con la misma metodología que el año anterior, se determinó el efecto
después de 15 semanas encontrando una eficacia alta en el control de
hongos en los suelos cubiertos con plástico, no encontrando alto efecto
en el control de Globodera pallida, aunque se observó reducción
de poblaciones de Pratylenchus penetrans y Meloidogyne fallax,
atribuyen la acción de control a las condiciones de anaerobiosis creadas
al incrementar el metabolismo del suelo con la incoporación de la materia
orgánica durante el proceso de fermentación; concluyen que el efecto de
control no se debe a las sustancias tóxicas volátiles desprendidas
durante la descomposición, ya que no se obtiene control de hongos al
incorporar brócoli sin plástico, reconocen que las sustancias volátiles
se producen pero no permanecen en el suelo el tiempo suficiente para que
actúen en el control de los patógenos, concluyendo que la incorporación
de materia orgánica puede ser importante pero es inconsistente, señalan
que los mecanismos de control están relacionados con la reducción de oxígeno
y la toxicidad de los productos químicos formados en condiciones de
anaerobiosis, que el bajo nivel de oxígeno no es por si solo suficiente
para el control de los patógenos, indicando que no es necesario que se
produzcan glucosinolatos para el control, que las diferencias de un año a
otro se deben a la cantidad de materia orgánica y existe el peligro de
que se recolonicen rápidamente los suelos por los patógenos, resultando
que la eficacia depende de la cantidad de materia orgánica, tipo de
cobertura y estado de nutrientes en el suelo. Estos resultados los vuelven
a publicar posteriormente (Blok et al. 2000), señalando únicamente
que el control no está relacionado con la temperatura por lo que se
diferencia claramente de la solarización, y puede aplicarse en lugares
donde la solarización y el encharcamiento no pueden ser aplicados, por lo
que lo consideran un nuevo método de control y lo denominan "biological
soil disinfestation". Perrin et al. (1998) encuentran que las
ectomicorrizas fueron de los hongos más sensibles a la solarización.
Eleftherohorinos y Giannopolitis (1999) indican que la eficacia de la
solarización puede estar relacionada con el balance de los compuestos
gaseosos (02,
CO2) (Rubin
y Benjamin 1984) y con la producción de acetaldehido y etileno siendo
efectivo en el control de un espectro amplio de malas hierbas, aunque es
menos efectivo en el control de las plantas perennes. Ploeg (2000)
encuentra que la combinación de solarización y biofumigación con bróculi
en cultivos de melón es eficaz en el control de M.incognita. Bello
et al. (2000c) señalan las diferencias entre solarización y
biofumigación en el control de nematodos en cultivos extensivos de
zanahoria, no siendo necesarias la aplicación de plástico y las altas
temperaturas, aunque ambas técnicas pueden ser complementarias.
DISCUSIÓN
Y CONCLUSIONES
Se define la biofumigación como
"la acción de las sustancias volátiles producidas en la
biodegradación de la materia orgánica en el control de los patógenos de
las plantas" (Bello et al. 2000). La técnica incrementa su
eficacia en el tiempo cuando forma parte de un sistema de producción
integrada. Se ha encontrado que, por lo general, cualquier materia orgánica
puede actuar como biofumigante, dependiendo su eficacia principalmente de
la dosis y del método de aplicación. En España existen buenos ejemplos
de su aplicación en cultivos de fresón en Andalucía y Valencia,
pimiento en Murcia y Castilla-La Mancha, cucurbitáceas en Valencia,
Castilla-La Mancha y Madrid, tomate en Valencia y Canarias, brasicas en
Valencia, platanera en Canarias, cítricos y frutales en Valencia, viñedos
en Castilla-La Mancha y flor cortada en Valencia (Bello et al.
1997, Bello y Melo 1998, Bello y Miquel 1998a,b, Bello et al. 1998,
Cebolla et al. 1999, García et al. 1999, Bello et al. 2000),
también se ha aplicado recientemente a cultivos de acelga en Madrid y
zanahoria en Andalucía y Valencia; los biofumigantes más utilizados han
sido estiércol de cabra, oveja y vaca, residuos de arroz, champiñón,
aceituna, brasicas y jardín (Fig. 2). Se ha obtenido una eficacia similar
a los fumigantes convencionales, al mismo tiempo que mejora las características
del suelo y la nutrición de la planta, siendo necesario diseñar una
metodología para cada situación. Su coste es mínimo puesto que las
diferencias con la aplicación de materia orgánica, práctica frecuente
en cualquier sistema de producción integrada, están en las características
de la materia orgánica y su método de aplicación. Se ha demostrado que
tiene la misma eficacia en el control de nematodos, hongos, insectos,
bacterias y plantas adventicias que los pesticidas convencionales,
pudiendo regular los problemas de virus al controlar los organismos
vectores (Bello et al. 2000).
La biofumigación es una técnica fácil de aplicación por
agricultores y técnicos, pues sólo se diferencia de la aplicación de
materia orgánica en la elección del biofumigante, que debe estar en vías
de descomposición y en el método de aplicación, que debe tener en
cuenta la necesidad de retener al menos durante dos semanas los gases
biofumigantes producidos en la biodegradación de la materia orgánica, ya
que su efecto en la mayoría de los casos no es biocida sino biostático,
por lo que es necesario prolongar en el tiempo su acción sobre los patógenos.
Se ha podido constatar, también, un marcado efecto herbicida. Se ha
demostrado que cualquier residuo agroindustrial o sus combinaciones que
presente una relación C/N comprendida entre 8-20 puede tener efecto
biofumigante, pudiéndose identificar con facilidad por el agricultor, ya
que produce un olor característico de amoniaco, aunque conviene recordar
que no solo los derivados del nitrógeno tienen efecto biofumigante, por
lo que sería recomendable previamente caracterizar de modo experimental
los residuos agroindustriales que quieren utilizarse como biofumigante
antes de su aplicación de modo comercial.
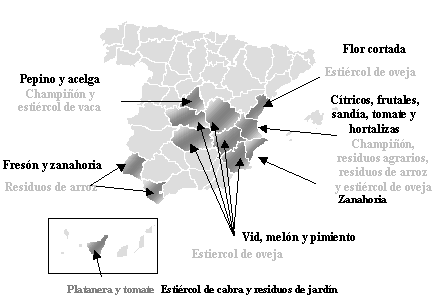
Figura
2. Áreas, cultivos y biofumigantes aplicados en España
Se debe procurar que durante el transporte y almacenaje en campo no se
pierdan los gases producidos en la biodegradación, cubriendo los montones
del biofumigante con plásticos hasta el momento de su aplicación. Se
recomienda la utilización de una dosis de 50 t ha-1,
aunque cuando los problemas de nematodos u hongos sean muy graves, se
deben aplicar 100 t ha-1,
dosis que se puede reducir mediante las técnicas de cultivo, como la
aplicación en surcos. Se debe distribuir el biofumigante uniformemente,
para que no aparezcan focos de patógenos que puedan crear problemas en el
cultivo. Una vez distribuido el biofumigante, se debe incorporar
inmediatamente al suelo mediante un pase de rotavator, dejando la
superficie del suelo lisa con la aplicación de la alomadora del rotavator.
Se riega, a ser posible por aspersión, hasta que se produce una saturación
del suelo, aunque se puede regar a manta o instalar goteros. Se cubre a
continuación con plástico para retener, durante al menos dos semanas,
los gases producidos en la biodegradación de la materia orgánica.
Cuando los suelos son poco profundos (< 30 cm), no es necesaria
la utilización de plástico, produciéndose la retención de los gases
con riegos frecuentes que mantengan una delgada capa de arcilla en la
superficie. Se recomienda efectuar la biofumigación cuando la temperatura
es superior a 20 ºC, aunque la temperatura no es un factor limitante. Se
puede combinar la biofumigación con la solarización, manteniendo el plástico
durante un período de un mes, aunque se ha observado que se produce una
disminución de la biodiversidad del suelo. Se recomienda la utilización
como biofumigantes de recursos locales, puesto que el principal factor
limitante de la biofumigación es el coste del transporte de los
materiales orgánicos. Se pueden producir algunos problemas en la
fertilización del suelo y la nutrición de la planta como fenómenos de
fitotoxicidad y deficiencia de nitrógeno, pero todo ello se puede
resolver con una fertilización adecuada.
Es recomendable alternar el empleo de residuos agrarios con abonos
verdes, especialmente de brasicas, empleando 5-8 kg m-2
de materia verde, aunque también se pueden aplicar combinaciones de
leguminosas con gramíneas. En el caso de la utilización de abonos verdes
cultivados en la misma parcela, deben utilizarse plantas de crecimiento rápido
para incorporar al menos a los 30 días de haberlo sembrado e impedir que
se incrementen las poblaciones de patógenos. El cultivo de brasicas después
de la biofumigación nos puede servir como bioindicadores de la posible
fitotoxicidad, puesto que la germinación de las semillas es sensible a
las sustancias fitotóxicas, al mismo tiempo que son muy sensibles a los
nematodos fitoparásitos y permiten detectar las áreas del cultivo donde
la biofumigación no es eficaz, pudiendo actuar como plantas trampa y, al
incorporarlas al suelo, como biofumigantes.
Los costes de la biofumigación pueden alcanzar el mismo valor que
el BM, especialmente cuando se aplican estiércoles de origen animal o
residuos agrarios que hay que traer desde grandes distancias, pero como
realmente se trata de la aplicación de una enmienda orgánica, que es una
práctica habitual en los sistemas producción integrada, se puede
considerar un coste cero. Los costes se pueden reducir aún más cuando se
utilizan abonos verdes, que no suelen superar los 300 $ EE.UU. por hectárea.
Puede aparecer alguna dificultad en los primeros tratamientos de
biofumigación, pero a medida que pasa el tiempo, el agricultor se va
familiarizando con el método, seleccionando las mezclas de biofumigantes
y estableciendo las dosis más eficaces, tanto desde el punto de vista de
su eficacia en el control de los patógenos como económico.
La solarización es un método que por si solo no es eficaz,
especialmente cuando se trata de controlar organismos móviles como
nematodos que por acción del calor se desplazan a zonas más profundas,
siendo incorporados de nuevo con las labores a la superficie del suelo. En
los casos donde la solarización ha sido eficaz, se trata por lo general
de suelos con alto contenido de materia orgánica (solarización más
biofumigación), o de suelos poco profundos. La solarización es eficaz
cuando se combina con biofumigación, durante dos meses, a una temperatura
ambiental superior a 40 ºC (Lacasa et al. 1999), aunque se
recomienda de 30 a 45 días durante los meses de julio y agosto, que es
cuando la temperatura del suelo alcanza temperaturas superiores a 50 ºC.
Hemos observado que se produce una pérdida en la biodiversidad del suelo.
La solarización resulta eficaz cuando se combina con bajas dosis de
fumigantes comerciales, reduciendo el impacto ambiental de estos
pesticidas, resultando una buena alternativa en los cultivos de fresón en
Huelva y zanahoria en Cádiz. La combinación de la solarización con
fumigantes como el metam sodio, a dosis muy reducidas (100 cc m-2),
es una práctica bastante frecuente en España. Los resultados son
equiparables a los de el BM (Bolívar 1999, Romero 2000).
Biofumigation, solarization and nematode
control
Summary. The action of gases
discharged by the decomposition of organic matter is studied for the
control of nematodes and soil-borne organisms. Effectiveness is similar to
conventional biofumigants, differing from solarization in that
temperatures over 30 ºC are not required. Therefore it can used in
different seasons of the year and in areas having low temperatures, as
well as on extensive crops. On the other hand, biofumigation acts in depth,
in the case of nematodes solving problems of vertical dynamics, which are
common to all mobile organisms, caused when the soil is heated by
solarization. Results of the application of biofumigation techniques in
extensive crops are shown under low temperature conditions and without the
application of plastic covers. This is different from solarization,
although both techniques can be complementary, increasing their
effectiveness in the case of phytopathogenic nematodes.
BIBLIOGRAFÍA
Abdel-Samie,F.S.; M.E. El-Bially. 1996. Azolla
and chemical as well as manual weed control methods in
two rice varieties. Annals of Agricultural Science, Moshtohor 34,
125-138.
Akiew, S.; P.R. Trevorrow; J.A. Kirkegaard. 1996. Mustard green manure
reduces bacterial wilt. ACIAR
Bacterial Wilt Newsletter 13, 5-6.
Al-Katib,K.; C.Libbey; R. Boydston. 1997. Weed suppression with Brassica
green manure crops in green
pea. Weed Science 45, 439-445.
Allen, L.H.; D.R. Sotomayor; D.W. Dickson; Z.Chen. 1997. Soil flooding
during the off-season as an alternative to methyl bromide. International
Research Conference on Methyl Bromide Alternatives and Emissions
Reductions, Nov. 3-5, 1997, San Diego, California, 94, 1-2.
Álvarez, M.; M. García; E. Treto; L. Fernández.. 1996. Efecto de
diferentes tipos de leguminosas
intercaladas sobre el rendimiento de la malanga. Cultivos Tropicales
17, 5-8.
Angus, J. F; P. A. Gardner; J. A. Kirkegaard; J. M. Desmarchelier. 1994.
Biofumigation: Isothiocyanates
released from Brassica roots inhibit growth of the take-all fungus.
Plant and Soil 162, 107-112.
Angus,J.F.; A.F. van Herwaarden; G.N. Howe. 1991. Productivity and break-crop
effect of winter growing
oilseeds. Aust.J.Exp.Agric. 31, 669-677.
Anju Kamra; H. S. Gaur. 1998. Control of nematodes, fungi and weeds in
nursery beds by soil solarization.
International Journal of Nematology 8, 46-52.
Antoniou P. P., E.C. Tjamos, C.G. Panagopoulos. 1997a. Reduced doses of
methyl bromide, impermeable
plastics and solarization against Fusarium oxysporum f.sp. cucumerinum
of cucumbers and Clavibacter
michiganensis subsp. michiganensis of tomatoes. Proceedings
of the 10th Mediterranean
Phytopathological Congress. Montpelier, France, 653-655.
Antoniou P. P., E.C. Tjamos, C.G. Panagopoulos. 1997b. Sensitivity of
propagules of Fusarium oxysporum
f.sp. cucumerinum, Verticillium dahliae, Clavibacter
michiganensis subsp. michiganensis to reduced doses
methyl bromide fumigation in combination with impermeable plastics. Phytopathologia
Mediterranean
(abstract In press).
Aponte, A.; A. Pérez; J. Tablante. 1992. Control de malezas y plagas en
tomate con la utilización de
residuos de cosecha. FONAIAP Divulga 9, 10-15.
Arias, M.; J. A. López-Pérez; R. Sanz; M. Escuer. 1999. Alternatives to
methyl bromide to control
nematodes in a cucumber-swiss chard rotation in greenhouses. Abstract of XXXI
Annual Meeting ONTA.
21-25 June, 1999, San Juan, Puerto Rico. Nematropica 29, 115.
Barker, K. R.; S. R. Koenning. 1998. Developing sustainable systems for
nematode management.
Ann.Rev.Phytopathol. 36, 165-205.
Bello, A. 1997. La retirada del bromuro de metilo como fumigante.
Consecuencias para la agricultura
española. Vida Rural 45, 70-72.
Bello, A. 1998. Biofumigation and integrated pest management. In:
A. Bello; J. A. González; M. Arias; R.
Rodríguez-Kábana (Eds). Alternatives to Methyl Bromide for the
Southern European Countries. Phytoma
España, DG XI EU, CSIC, Valencia,Spain, 99-126.
Bello, A.; M. Escuer; M. Arias. 1994. Nematological problems, production
systems and Mediterranean
environments. Bulletin OEPP 24, 383-391.
Bello, A.; M. Escuer; J. A. López-Pérez; M. Arias. 1996. Ecología del
suelo y su interés agronómico en el
control de nematodos. IV Congreso de la Sociedad Española de la
Ciencia del Suelo. Lérida, España,
339-344..
Bello, A.; M. Escuer; M. A. Pastrana. 1995. Nematodos fitoparásitos de la
alcachofa. Horticultura 165,
535-538.
Bello, A.; M. Escuer; R. Sanz; J. A. López-Pérez; P. Guirao. 1997.
Biofumigación, nematodos y bromuro
de metilo en el cultivo de pimiento. In: A. López; J. A. Mora (Eds). Posibilidad
de Alternativas Viables al
Bromuro de Metilo en Pimiento de Invernadero. Consejería de
Medioambiente,Agricultura y Agua, Murcia,
España, 67-108.
Bello, A., M. Escuer; J. Tello. 1999. Problemas nematológicos de los
cultivos de Guatemala y su manejo
agronómico. Abstracts of the XXXI Annual Meeting ONTA, June 21-25,
1999, San Juan, Puerto Rico.
Nematropica 29, 116-117.
Bello A., J.A. González, J. Pérez Parra, J. Tello. 1997. Alternativas
al Bromuro de Metilo en Agricultura.
Junta Andalucía, Sevilla 44/97, 192 pp.
Bello A., J.A. González, M. Arias, R. Rodríguez-Kábana. 1998. Alternatives
to Methyl Bromide for the Southern
European Countries. Phytoma-España, DG XI EU, CSIC, Valencia, Spain,
404 pp.
Bello, A.; J. A. López-Pérez; L. Díaz-Viruliche; L. de León; R. Sanz;
M. Escuer. 1999a. Local resources as
methyl bromide alternatives in nematodes control. Abstracts of the XXXI
Annual Meeting ONTA, June 21
25, San Juan, Puerto Rico. Nematropica 29, 116.
Bello, A.; J.A. López-Pérez; L. Díaz-Viruliche; R.Sanz; M.Arias. 1999b.
Bio-fumigation and local resources
as methyl bromide alternatives. Abstracts 3rd
International Workshop "Alternatives to Methyl Bromide for
the Southern European Countries, 7-10 December, Heraclion, Creta,
Grecia, 17 p.
Bello, A.; J.A. López-Pérez; L. Díaz-Viruliche; R.Sanz; M.Arias. 2000a.
Biofumigation and local resources
as methyl bromide alternatives. Nematropica. (en prensa)
Bello, A.; J.A. López-Pérez; R.Sanz; M.Escuer; J.Herrero. 2000b.
Biofumigation and organic amendments.
Regional Workshop on Methyl Bromide Alternatives for North Africa and
Southern European Countries,
United Nations Environment Programme (UNEP), Francia, 113-141.
Bello, A.; J.A. López-Pérez; L. Díaz-Viruliche; R.Sanz. 2000c.
Biofumigation, solarization and nematode
control. XXV International Nematology Symposium, April 2-7, 2000,
Herzliya, Israel.
Bello, A.; J.A. López-Pérez; L. Díaz-Viruliche; J. Tello. 2000.
Alternativas al bromuro de metilo como
fumigante del suelo en España. In: R. Labrada (Ed.) Report on
Validated Methyl Bromide Alternatives.
FAO, Rome, 13 pp (in press).
Bello, A.; M.J. Melo. 1998. Reducción de las poblaciones de nematodos con
técnicas alternativas al bromuro de metilo. In: Memoria de Actividades
1998, Resultados de Ensayos Hortícolas, Generalitat Valenciana,
Fundación Caja Rural de Valencia, 347-350.
Bello, A.; E. Miquel. 1998a. Control nematodos por biofumigación. In: Memoria
de Actividades 1998, Resultados de Ensayos Hortícolas, Generalitat
Valenciana, Caja Rural de Valencia, 351-352.
Bello, A.; E. Miquel. 1998b. Control nematodos por biofumigación en
cultivo de col china. In: Memoria de Actividades 1998, Resultados de
Ensayos Hortícolas, Generalitat Valenciana, Caja Rural, Valencia,
353-354.
Bello A.; J. Tello. 1998. El bromuro de metilo se suprime como fumigante
del suelo. Phytoma-España 101, 10-21.
Beltrán, L. 1997. ¿La alelopatía; ciencia o fenómeno? Cultivos
Tropicales 18, 47-58.
Blok, W.J.; J.G. Lamers; A. J. Termorshuizen; G.T: Bollen. 2000. Control
of soil-borne plant pathogens by incorporating fresh organic amendments
followed by tarping. Phytopathology 90, 253-259.
Blok, W.J.; C.P. Slomp; A.J. Termorshuizen; J.A. Lamers. 1998. Control of
soil-borne pahogens by inducing soil anaerobiosis. Phytoparasitica
26, 244.
Bolívar, J.M. 1999. Current status of methyl bromide alternatives in
Spain. 3rd
International Workshop Alternatives to Methyl Bromide for the Southern
European Countries. 7-10 December, Creta (Greece), 139-140.
Borek,V.; L.R.Elberson; J.P.McCaffrey; M.J.Morra. 1997. Toxicity of
rapeseed meal and methyl isothiocyanate to larvae of the black vine weevil
(Coleoptera: Curculionidae). J.Econ.Entom.90, 109-112.
Bowers, J.H.; J.C. Locke. 1997. Effect of botanical extracts on soil
populations of Fusarium and other soil-borne pathogens. International
Research Conference on Methyl Bromide Alternatives and Emissions
Reductions, Nov. 3-5, 1997, San Diego, California, 2, 1-4.
Boydston,R.A.; A. Hang. 1995. Rapeseed (Brassica napus) green
manure crop supresses weeds in potato (Solanum tuberosum). Weed
Technology 9, 669-675.
Brown, P.D.; M.J. Morra. 1997. Control of soil-borne plant pests using
glucosinlate-containing plants. Advan. Agron. 61, 167-231.
Calderón, L.; F. Solís; E. Trabanino; E. Barillas; E. García. 2000. The
effect of alternative treatments as methyl bromide for nematode control in
different crops: 1998-1999. Abstract. XXXII Annual Meeting of ONTA,
16-20 abril, Auburn, Alabama, O-7, 48.
Candole, B.L.; C.S. Rothrock. 1997. Characterization of the supressiveness
of hairy vetch-amended soils to Thielaviopsis basicola. Phytopathology
87, 197-202.
Canullo, G. H.; R. Rodríguez-Kábana; J. W. Kloepper. 1992a. Changes in
populations of microorganisms associated with the application of soil
amendments to control Sclerotium rolfsii Sacc. Plant and Soil
144, 59-66.
Canullo, G. H.; R. Rodríguez-Kábana; J. W. Kloepper. 1992b. Changes in
soil microflora associated with control of Sclerotium rolfsii by
furfuraldehyde. Biocontrol Science and Technology 2, 159-169.
Cebolla V.; R. Bartual; A. Giner; J. Busto; F. Pomares; S. Zaragoza; J.J.
Tuset; P.Caballero; M. Mut; B. Cases; M.D. de Miguel; P. Fombuena; J.V.
Maroto; A. Miguel; J.L. Porcuna. 1999. Chemical and non chemical
alternatives to methyl bromide in the area of Valencia. 3rd
International Workshop Alternatives to Methyl Bromide for the Southern
European Countries. 7-10 December, Creta (Greece), 141-145.
Chan M.Y.K.; R.C. Close. 1987. Aphanomyces root rot of peas. 3. Control by
the use of cruciferous amendments. N.Z.J.Agric.Res. 30, 225-233.
Ciuberkis, S. 1997. Ecological significance of long term fertilization
with farmyard manure and soil reaction on weed flora. In Integrated
Plant Protection: Achievements and Problems. Proceedings of the Scientific
Conference Devoted to the 70th
Anniversary of Plant Protection Science in Lithuania, Dotnuva-Akademija,
Lithuania, 7-9 September 1997, 184-187.
Cloutier,D.C.; R.Marcotte; M.L. Leblanc. 1994. Evaluation du potentiel des
cultures intercalires et des engrais verts contre les populations de
mauvaises herbes. In Maitrise des adventices par voie non chimique.
Communications de la Quatrieme Conference Internationale, Dijon, France,
5-9 july 1993. 2, 201-205.
Cook, R. J.; K. R. Barker (Eds). 1983. The Nature and Practice of
Biological Control of Plant Pathogens. St. Paul American
Phytopathological Society, 539 pp
Culbreath, A. K.; R. Rodríguez-Kábana; G. Morgah-Jones. 1985. The use of
hemicellulosic waste matter for reduction of the phytotoxic effects of
chitin and control of root-knot nematode. Nematropica 15, 49-75.
Dhanapal, G.N.; P.C: Struik; P.C.J.M. Timmermans; S.J. ter Borg. 1998.
Postemergence control of broomrape with natural plant oils. Journal of
Suistanable Agriculture 11, 5-12.
Díaz-Viruliche, L.; A. Pinilla; J.A. López-Pérez; A. Bello. 2000.
Biominerales y efecto biofumigante de los abonos verdes. XXXII Annual
Meeting of the Organization of Nematologist of Tropical American (ONTA),
April 16-20, 2000, Auburn, Alabama, USA. 51.
Duniway, J.M.; C.L. Xiao; H.Ajiwa; W.D. Gubler. 1999. Chemical and
cultural alternatives to methyl bromide fumigations of soil for strawberry.
Annual Intern. Research Conference on Methyl Bromide Alternatives and
Emission Reductions, Nov. 1-4, 1999, San Diego, California, 2, 2 pp.
Duplessis, M. C. F.; W. Kroontje. 1964. The relationship between pH and
ammonia equilibrium in soil. Proc.Soil Sci.Soc.America 28, 751-754.
Dyck, E.; M. Liebman; M.S.Erich. 1995. Crop-weed interference as
influenced by a leguminous or synthetic fertilizer nitrogen source: I.
Doublecropping experiments with crisom clover, sweet corn and lambsquaters.
Agriculture, Ecosystems and Environment 56, 93-108.
Eberlein,C.V.; M.J.Morra; M.J.Guttieri; P.D. Brown; J. Brown. 1998.
Glucosinolate production by five field-grown Brassica napus cultivars used
as green manures. Weed Technology 12, 712-718.
Edwards,J.H.; R.H. Walker. 1997. Using organic residuals on highly
erodible soil. BioCycle 38, 56-57.
Edwards,J.H.; R.H. Walker; W.B. Webster. 1994. Effect of non-composted
organic waste as residues on cotton yields. Proceedings Beltwide Cotton
Conferences, January 5-8, San Diego, California. National Cotton Council,
1561-1563.
Elberson, L.R.; V. Borek; J.P. McCaffrey; J.Morra. 1996. Toxicity of
rapeseed meal-amendment soil to wireworms, Limonius californicus (Coleoptera:
Elasteridae). J.Agric.Entomol. 13, 323-330.
Eleftherohorinos, I.G.; C.N. Giannopolitis. 1999. Alternatives to methyl
bromide for the control of weeds in
greenhouses and seed beds. Proceedings of International Workshop "Alternatives
to Methyl Bromide for the Southern European Countries", Heraklio,
Creta, Grecia, 34-36.
Elena, K.; E.J. Paplomatas; N. Petsikos-Panayotarou. 1999. Bio-disinfestation:
an alternative method to control soil pathogens. Proceedings of
International Workshop "Alternatives to Methyl Bromide for the
Southern European Countries", Heraklio, Creta, Grecia, 81-82.
Elena K., E.C. Tjamos.1992. Control of Fusarium wilt of carnation by soil
solarization singly or in combination with fungal or bacterial biocontrol
agents. pages 75-78. In: E. C. Tjamos, G.C. Papavizas,
R.J. Cook (Eds). Biological Control of Plant Diseases. Progress and
Challenges for the Future., NATO ASI Series A, Life Sciences, Plenum Press,
vol. 230.
Eno, C. F.; W. G. Blue; J. M. Jr. Good. 1955. The effect of anhydrous
ammonia on nematodes, fungi, bacteria, and nitrification in some Florida
soils. Proc. Soil Science Society of America 19, 55-58.
Fernández, C.; R.Rodríguez-Kábana; J.W. Kloepper. 2000. Approaches to
measuring microbial contributions to soil suppressiveness by measuring
soil enzymes. Abstract. XXXII Annual Meeting of ONTA, 16-20 April, Auburn,
Alabama, W-1, 20.
Fieldsend,J.; G.F.J. Milford. 1994. Changes in glucosinolates during crop
development in single- and doble-low genotypes of winter oilseed rape (Brassica
napus): I. Production and distribution in vegetative tissues and
developing pods during development and potential role in the recycling of
sulphur within the crop. Ann.Appl.Biol. 124, 531-542.
Fravel D.R. 1988. Biocontrol Of Verticillium wilt of eggplant and potato.
Pages 487-492. In : E.C. Tjamos, C.H. Beckman (Eds). Vascular Wilt
Diseases of Plants. Springer-Verlag, Berlin. 590 pp.
Galper, S.; E. Cohn; Y. Spiegel; Y. Chet. 1991. A collagenolytic fungus,
Cunninghamella elegans, for biological control of plant parasitic
nematodes. J.Nematol. 23, 269-274.
Gamliel A.; M.Austerweil; G.Kritzman, I.Pérez. 1999. Combined organic
amendments with soil heating to control soil-borne plant pathogens. Annual
Intern. Research Conference on Methyl Bromide Alternatives and Emission
Reductions, Nov. 1-4, 1999, San Diego, California, 27, 1-2 pp.
Gamliel A., J. Katan. 1991. Involvement of fluorescent Pseudomonas and
other micro-organisms in increased growth response of plants in solarized
soils. Phytopathology 81, 494-502.
Gamliel, A.; J. J. Stapleton. 1993. Characterization of antifungal
volatile compounds evolved from solarized soil amended with cabbage
residues. Phytopathology 83, 99-105.
García, S.; F. Romero; J. J. Sáez; A. de Miguel; C. Monzó; V. Demófilo;
M. Escuer; A. Bello. 1999. Problemática de la replantación de
melocotoneros en terrenos arenosos en la comarca de La Rivera (I).
Comunitat Valenciana Agraria 13, 43-49.
García,R.; J.E. Poot. 1997. Cropping systems
and soil-borne diseases in México. XXIX
Annual Meeting, June 29th to July 4th, Cancún, México, 23 p.
Garibaldi, A.; M. L. Gullino. 1991. Soil solarization in Southern European
countries, with emphasis on soilborne diseases control of protected crops.
In: J. Katan; J. E. de Vay (Eds). Solarization. CRC Press Boca Raton Ann
Arbor Boston, London, UK, 227-235.
Golpa Krishnan; D.L. Holshouser; S.J. Nissien. 1998. Weed control in
soybean (Glycine max) with green manure crops. Weed technology 12, 97-102.
Gooday, G. W. 1990. The ecology of chitin degradation. In: K. C. Marshall
(Eds). Advances in Microbial Ecology, Vol. II. Plenum Press, New
York, USA, 387-430.
Greenberger A., A. Yogev, J. Katan. 1987. Induced suppressiveness in
solarized soils. Phytopathology 77, 1663-1667.
Gyldenkaerne, S.; D. Yohalem; E. Hvalzøe. 1997. Production of Flowers and
Vegetables in Danish Greenhouses Alternatives to Methyl Bromide. Ministry
of Environment and Energy, Denmark, Danish Environmental Protection Agency,
35 pp.
Hewlett, T.E.; D.W. Dickson. 2000. Efficacy of tannis for control of root-knot
nematodes. Abstract. XXXII Annual Meeting of ONTA, 16-20 abril, Auburn,
Alabama, O-29, 57.
Hintzsche,E.; B.Pallut. 1995. Increasing occurrence of creping thistle.
Zunehmendes Auftreten der Ackerkratzdistel. PSP Pflanzenschutz Praxis 3,
23-25.
Hoitink, H. A. 1988. Basis for the control of soilborne plant pathogens
with composts. Ann.Rev.Phytopathol. 24, 93-114.
Hoitink, H.A. 1997. Disease suppressive compost as substitutes for methyl
bromide. International Research Conference on Methyl Bromide Alternatives
and Emissions Reductions, Nov. 3-5, 1997, San Diego, California, 1, 1-2.
Horiuchi, S.; M. Hori; S. Takashi; K. Shimuzu. 1982. Factors responsible
for the development of clubroot-suppressing effect in soil solarization.
Bull.Chugoku Nat.Agric Exp.Stn. E20, 25.
Huebner, R. A.; R. Rodríguez-Kábana; R. M. Patterson. 1983.
Hemicellulosic waste and urea for control of plant parasitic nematodes:
effects on soil enzyme activities. Nematropica 13, 37-45.
Hunter, B.B.; T. Hall; M.T. Lyons; T.K. Bell. 1997. Field application of
sewage and spent mushroom compost in conjunction with Basamid, a fumigant,
to control the root pathogen, Cylindrocladium scoparium, in forest nursery
soils. International Research Conference on Methyl Bromide Alternatives
and Emissions Reductions, Nov. 3-5, 1997, San Diego, California, 45, 1-4.
Jacobs, J. J.; A. Engelberts; A. F. Croes; G. J. Wullems. 1994. Thiophene
synthesis and distribution in young developing plants of Tagetes patula
and Tagetes erecta. Journal of Experimental Botany 45, 1459-1466.
Katan, J. 1981. Solar heating (solarization) of soil for control of soil-borne
pests. Annu.Rev.Phytopathol. 17, 211.
Katan, J.; G. Fishler; A. Grinstein. 1983. Short and long-term effects of
soil solarization and crop sequence on Fusarium wilt and yield of cotton
in Israel. Phytopathology 73, 1215-1219.
Katan, J.; J. E. de Vay (Eds). 1991. Solarization. CRC Press Boca Raton
Ann Arbor, Boston, London, 267 pp
Katan J., J.E. de Vay, A. Greenberger. 1989. The biological control
induced by soil solarization. In: E.C.Tjamos, C.H. Beckman (Eds), Vascular
Wilt Diseases of Plants, 493-499.
Kim K.K., D.R. Fravel, G.C. Papavizas. 1988. Identification of a
metabolite produced by Talaromyces flavus as glucose oxidase and its role
in the biocontrol of Verticillium dahliae. Phytopathology 78, 488-492.
Kim, K. D.; S. Nemec; G. Musson. 1996a. Control of Phytophtora stem rot of
pepper with compost and soil amendment in the greenhouse. International
Research Conference on Methyl Bromide, Alternatives and Emissions
Reductions. Methyl Bromide Alternatives Outreach, US Dept.of Agriculture,
Florida, USA 100, 1-3.
Kim, K. D.; S. Nemec; G. Musson. 1996b. Effect of compost and soil
amendments on soil microflora an Phytophtora stem rot of pepper.
International Research Conference on Methyl Bromide, Alternatives and
Emissions Reductions. Methyl Bromide Alternatives Outreach, US Dept.of
Agriculture, Florida, USA 101, 1-3.
Kim Kilung; Park Kwangho. 1997. Weed management using a potential
allelopathic crop. Korean Journal of Weed Science 17, 80-93.
Kirkegaard, J.A.; J.F. Angus; P.A. Gardner;
H.P. Cresswell. 1993a. Benefits of brassica break crops in the Southeast
wheatbelt. Proc. 7th Aust. Agron. Cons. Adelaide, 19-24 Sept., 282-285.
Kirkegaard, J. A.; J. Gardner; J. M.
Desmarchelier; J. F Angus. 1993b. Biofumigation using Brassica species to
control pest and diseases in horticulture and agriculture. In: N. Wrather;
R. J. Mailes (Eds). Proc. 9th Australian Research Assembly on Brassicas (Wagga
Wagga) . 77-82.
Kirkegaard, J.A.; M. Sarwar. 1998. Biofumigation potential of brassicas: I.
variation in glucosinolate profiles of diverse field-grown brassicas.
Plant and Soil 201, 71-89.
Kirkegaard, J.A.; P.T.W. Wong; J.M. Desmarchelier. 1996. In vitro
supression of fungal root pathogens of cereals by Brassica tissues. Plant
Pathol. 45, 593-603.
Kjaer,A. 1976. Glucosinolates in cruciferae. In: J.G.Vaughan, A.J.Macleod,
B.M.G.Jones (Eds). The Biology and Chemistry of the Cruciferae, Academic
Press, London, 207-219.
Kodama, T.; T. Fukui. 1982. Application of solar heating with plastic-film
mulching in the outdoor field for control of Fusarium wilt of strawberries.
Ann.Phytopatol.Soc.Jpn.48, 699. 48, 699-699.
Lacasa A., P. Guirao, M.M. Guerrero, C. Ros, J.A. López-Pérez, A. Bello,
P. Bielza. 1999. Alternatives to methyl bromide for sweet pepper
cultivation in plastic greenhouses in south east. 3rd International
Workshop Alternatives to Methyl Bromide for te Southern European Countries.
7-10 December, Creta (Greece), 133-135.
Lacayo, C.H.M.; C.C. Gómez; C.G. Gutiérrez; Q. Díez. 1999. Control de
Sitophilus zeamais (Coleoptera: Cucurculionidae) con CO2 obtenido de
diferentes fuentes orgánicas en silos metálicos de cuatro hembras. VI
Congreso Internacional de Manejo Integrado de Plagas. Sept 29-oct.4,
Acapulco, México, 95 p.
Lazarovits, G.; K.Conn; G.Kritzman. 1997. High nitrogen containing organic
amendments for the control of soilborne plant pathogens. International
Research Conference on Methyl Bromide Alternatives and Emissions
Reductions, Nov. 3-5, 1997, San Diego, California, 3, 1-2.
Li Shanlin; You Zhenguo; Liang; Duxiang; Li Sunrong; Wang Nanjin. 1997.
Extraction and separation of allelochemicals in wheat and its herbicidal
efficacy on Imperata cylindrica. Acta Phytophylacica Sinica 24, 81-84.
Mahendra Singh; R. Samar; G. L. Sharma. 1998. Effect of various levels of
organic carbon on the development of Pasteuria penetrans on Meloidogyne
incognita. Indian J.Nematol. 28, 72-76.
Mathew, G.; D. Alexander. 1995. Influence of intercropped green manure
crops on weed pressure and grain yield of semi dry rice. Madrás
Agricultural Journal 82, 66-67.
Matthiesen, J. N.; J. A. Kirkegaard. 1993. Biofumigation, a new concept
for 'clean and green' pest and disease control. Western Australian Potato
Grower October, 14-15.
MBTOC. 1997. Report of the Technology and Economic Assesment Panel. UNEP,
Nairobi, Kenia, 221 pp.
MBTOC. 1998. Report of the Methyl Bromide Technical Options Committee.
1998 Assessment of Alternatives to Methyl Bromide, UNEP, Nairobi, Kenia,
354 pp
Mian, I. H.; G. Godoy; R. Rodríguez-Kábana; G. Morgah-Jones. 1982.
Chitin amendments for control of Meloidogyne arenaria in infested soil.
Nematropica 12, 71-84.
Mian, I. H.; R. Rodríguez-Kábana. 1982a. Soil amendments with oil cakes
and chicken litter for control of Meloidogyne arenaria. Nematropica 12,
205-220.
Mian, I. H.; R. Rodríguez-Kábana. 1982b. Organic amendments with high
tannin and phenolic contents for control of Meloidogyne arenaria in
infested soil. Nematropica 12, 221-234.
Michel, V.V.; T.W. New. 1996. Effect of a soil amendment on the survival
of Ralstonia solanacearum in different soils. Phytopathology 88, 300-305.
Michel, V.V.; J.F. Wang; D.J. Midmore; G.L. Hertman. 1997. Effects of
intercropping and soil amendment with urea and calcium oxide on the
incidence of bacterial wilt of tomato and survival of soil-borne
Pesudomonas solanacearum in Taiwan. Plant Pathology 46, 600-610.
Mojtahedi, H; G. S. Santo; A.N. Hang; J.H. Wilson. 1991. Suppression of
root-knot nematode populations with selected rapeseed cultivars as green
manure. J. Nematol. 23, 170-174.
Munnecke, D.E. 1984. Establishment of microorganisms in fumigated avocado
soil to attempt to prevent reinvasion of the soils by Phytophtora
cinnamoni. Trans. Br. Mycol. Soc. 83, 287.
Nanda,R.; S.C. Bhargava, D.P.S. Tomar; H.M. Rawson. 1996. Phenological
development of Brassica campestris, B. juncea, B. napus and B. carinata
grown in controlled environments and from 14 sowing dates in the field.
Field Crops Res. 46, 93-103.
Nietschke, B.S. 1996. Cultural weed management of wild oats. In Wild Oats,
Annual Ryegrass and Vulpia. Proceedings of a Workshop held at Orange, New
South Wales, Australia on 26-27 March 1996, P.
Dowling; R.Medd (Eds) Plant Protection Quaterly 11, 187-189.
Noble, R.R.P.; C.E. Sams. 1999. Biofumigation as an alternative to methyl
bromide for control of white grub larvae. Annual Intern. Research
Conference on Methyl Bromide Alternatives and Emission Reductions, Nov.
1-4, 1999, San Diego, California, 92, 3 pp.
Oliveira, A.E.A.; V.M. Gomes; M.P. Sales; K.V.S. Fernandes; C.R. Carlini;
J. Xavier-Filho. 1996. The toxicity of jack bean (Cannavalia ensiformis
(L.) D.C.) can a toxin to plant pathogenic fungi. Revista Brasileira de
Biologia 59, 59-62.
Otara, C.O.; P.K. Ndalut. 1999. Application of Conyza floribunda
extractives to control soil pathogens in tomato fields. Annual Intern.
Research Conference on Methyl Bromide Alternatives and Emission
Reductions, Nov. 1-4, 1999, San Diego, California, 20, 1 p.
Pandey, D.K. 1994a. Inhibition of salvinia (Salvinia molesta Mitchell) by
parthenium (Parthenium hydterophorus L.). I. Effect of leaf residue and
allelochemicals. Journal of Chemical Ecology 20, 3111-3122.
Pandey, D.K. 1994b. Inhibition of salvinia (Salvinia molesta Mitchell) by
parthenium (Parthenium hydterophorus L.). I. Relative effect of flower,
leaf, stem and root residue on salvinia and paddy. Journal of Chemical
Ecology 20, 3123-3131.
Papavizas, G.C.; C.B. Davey. 1960. Rhizoctonia disease of bean as affected
by decomposing green plant materials and associated microfloras.
Phytopathology 60, 516-522.
Parker, N.; A. C. Haywards; G. R. Stirling. 1988. Effect of chitinolytic
soil bacteria on root-knot nematode eggs. Fifth International Congress of
Plant Pathology, Abstracts of Paper, Kyoto , 157.
Perrin, R.; P. Camporota; M.L. Soulas; B. Le Bihan. 1998. The management
of mycorrhizal symbiosis and solarization as an alternative to soil
fumigation. In: A. Bello; J. A. González; M. Arias; R. Rodríguez-Kábana
(Eds). Alternatives to Methyl Bromide for the Southern European
Countries. DG XI EU, CSIC, Valencia, Spain, 301-310.
Pimentel, D.; L. McLaughlin; A. Zeep; B. Lakistan; T.
Kraus; P. Kleinman; F. Vancini; W. J. Roach; E. Graap; W. S. Keeton; G.
Selig. 1993. Environmental and economic effect of reducing pesticide use
in agricultura. Agriculture, Ecosystems and En

